
1218
0
详细信息
药品审评中心官网查询入口
药品审评进度是医药研发人员每日关注的核心事项。为保障信息公开透明,CDE药审中心提供覆盖各注册分类及申请类型的审评审批进度查询服务,涵盖从承办、新报任务(含NDA序列的离开队列时间、药理毒理用时、临床用时、药学用时)、离开新报任务、CDE寄发通知、补充资料任务、离开补充任务、药监局审批、审批完毕、制证时间到批准发件等全流程关键节点。
然而,CDE官网改版后,许多用户对查询技巧并不熟悉。为此,笔者整理了两种查询方法及实操案例,希望能帮助大家提升信息检索效率。
方法一、CDE药品审评中心Center for Drug Evaluation(贯穿药品上市前阶段)
诸位可通过CDE药品审评中心官网的"受理目录浏览"和"新报任务公示"板块,查询药品注册申请的受理概况及各注册分类序列的审评审批进度。此外,申请人还可登录"申请人之窗"或使用"进度查询"功能,查看具体品种的受理及审评审批状态。
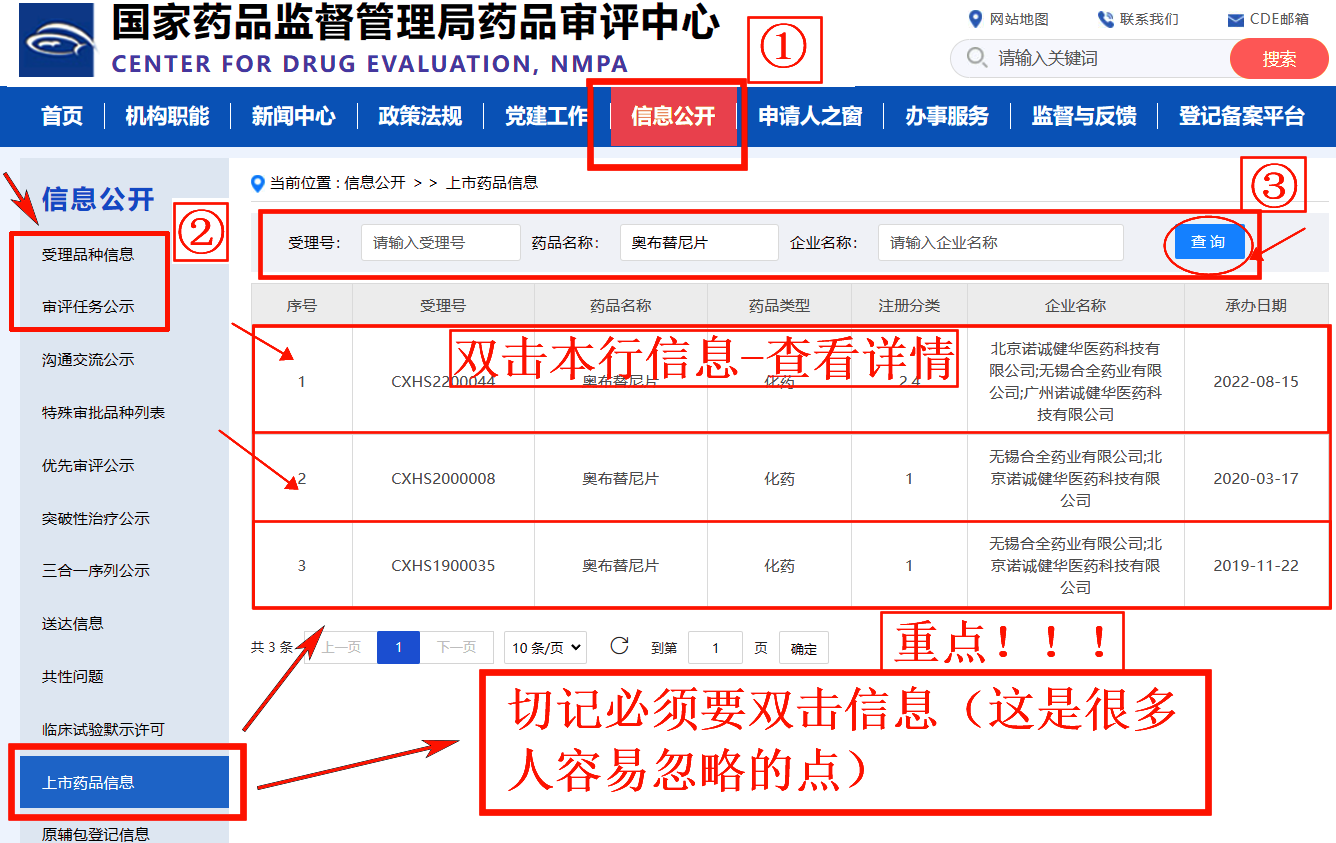
查询步骤:登录CDE官网首页→点击"信息公开"→选择"受理品种信息"或"审评任务公示"
官网查询入口:www.cde.org.cn
重要提示:如需查看药品上市申请的技术审评报告,需双击上市药品信息栏目中对应的药品名称。
方法二、中国药品审评数据库(行业必备高效工具)
功能理解:以业内常用的(摩熵医药)中国药品审评数据库举例,这个数据库是综合国家药监局与药审中心等多个部门的多个官方数据库整合而成,收录了药品审评中心公布的全部受理号及其办理状态,包括国内新药注册申报、补充申请、进口等情况,同时收录了优先审评、突破性治疗等特殊审评品种,并经过系统整理,深度加工,可以了解潜在竞争产品及其目前状况,预测竞品上市时间,提供决策支持。 本数据库支持多类型、多角度检索,查询方式灵活,可供分析查询的维度包括申报药品名称、申报企业、申报类型、注册分类、治疗领域、审评审批状态、审评序列与序号、审评结论及相应的变化时间等多种检索方式,并能快速筛选出优先审评、重大专项、特殊审评品种及一致性评价品种等。另外在结果中增加的审评时间轴功能包含了各个主要审评状态的统计信息,直观呈现目标药品的审评进度。
实战案例:药品审评进度的查询、筛选、分析与变化监测
在摩熵医药药品审评数据库中,可通过药品名称、企业名称、受理号、批准文号、靶点、适应症等字段检索目标品种,亦可借助注册类型、国产/进口属性、各节点日期、申报内容、办理状态、一致性评价、地区、是否独家、申报企业数量、获批企业数量及药品基本属性等条件进行多维度筛选。
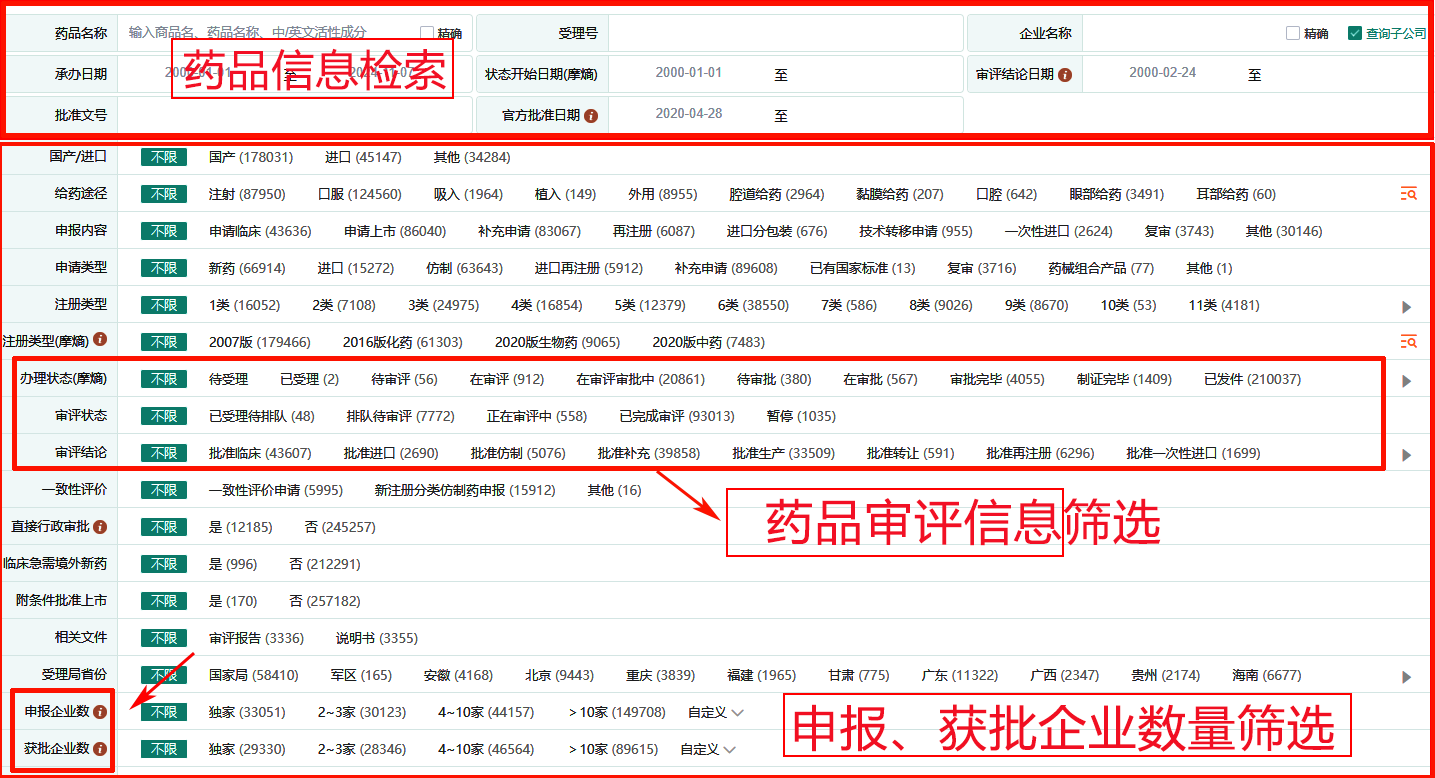
检索步骤:访问摩熵医药官网→进入"数据库"→选择"药品研发"→点击"中国药品审评"
然后在上图搜索界面中,我们查找到符合条件药品后,通过点击即可查看该受理号对应的基本信息、审评概况、审评时间轴、研发历程时间轴,以及专利、招投标等相关联信息(如下图)。
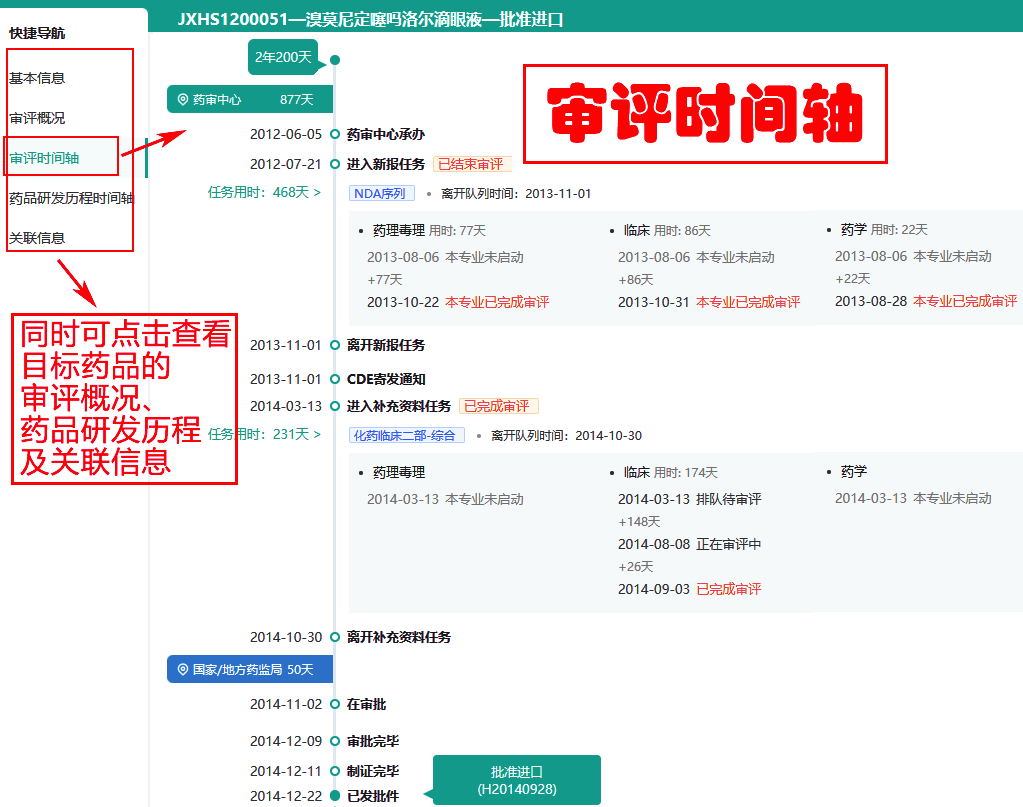
在上图审评时间轴界面中,我们可清晰查看承办日期、NDA排队序列状态、离开队列时间、药理毒理审评耗时、临床审评耗时、药学审评耗时、CDE寄发通知时间、补充资料任务时间、药监局审批完毕时间、制证时间及批准发件时间等全流程关键节点信息。
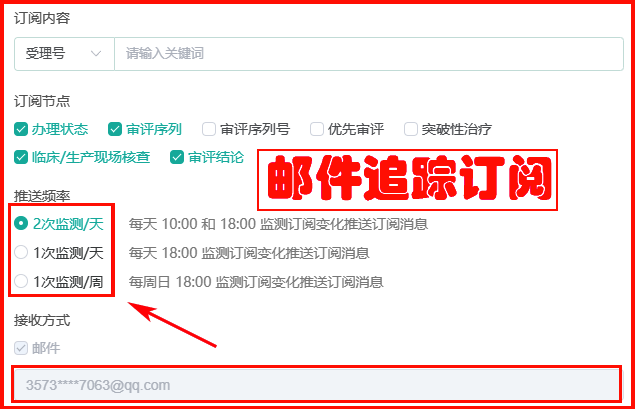
重点目标药品需要跟踪监测其审评进度变化,只需开通邮件订阅功能接收消息提醒即可。订阅时需勾选关注的审评节点及推送频率,并填写接收邮箱地址即可完成设置。
以上即为药品审评进度查询的两种常用方法。都是一些基础必修课,不要求大家对其多么精通造诣,但需具备快速检索的能力,熟悉这些平台及工具,如此方能在有限的生命中,腾挪出更多的时间,于笔者而言,此文亦是对理查德·费曼"以教促学"理念的践行。
随机推荐
最新推荐

