
407
0
美国FDA的各类数据该如何查看呢?(知识点梳理)
FDA的各类数据该如何查看呢?下面笔者就系统阐述FDA药品五大核心信息资源的查询路径与应用策略,以提升信息获取效率与决策科学性。
推荐指数:
详细信息
美国FDA数据查询
美国食品药品监督管理局(FDA)作为全球药品监管的标杆机构,建立了系统化、多层次的信息公开与数据查询体系。其发布的各类数据库不仅为药品研发、注册申报和临床用药提供了权威依据,也成为国际医药企业进行市场准入评估与竞争情报分析的核心工具。
那么,FDA的各类数据该如何查看呢?下面笔者就系统阐述FDA药品五大核心信息资源的查询路径与应用策略,以提升信息获取效率与决策科学性。
FDA核心板块数据
对于药研人而言,FDA新获批药物的各类审批文件是其关注重点对象,其中便包含说明书与审评报告。
若聚焦药学评价内容,可登录FDA官网,点击“Product Quality Review”板块查看。
若关注临床前药理学、毒理学评价以及临床试验相关信息,则可下载“Multi-Discipline Review”文件。这份文件虽未涵盖试验报告全文,但汇总了所有试验的摘要,同时还包含试验类型、实验动物种属、给药剂量、检测指标以及阳性发现等关键信息。
宝藏文件“Risk Assessment and Risk Mitigation Review(s)”,这里面详细阐述了对应药物适应症的当前市场需求、现有治疗方案,以及新获批药物的优势与不足,是撰写综述类文章的优质参考资料。
FDA数据查询技巧&工具利用
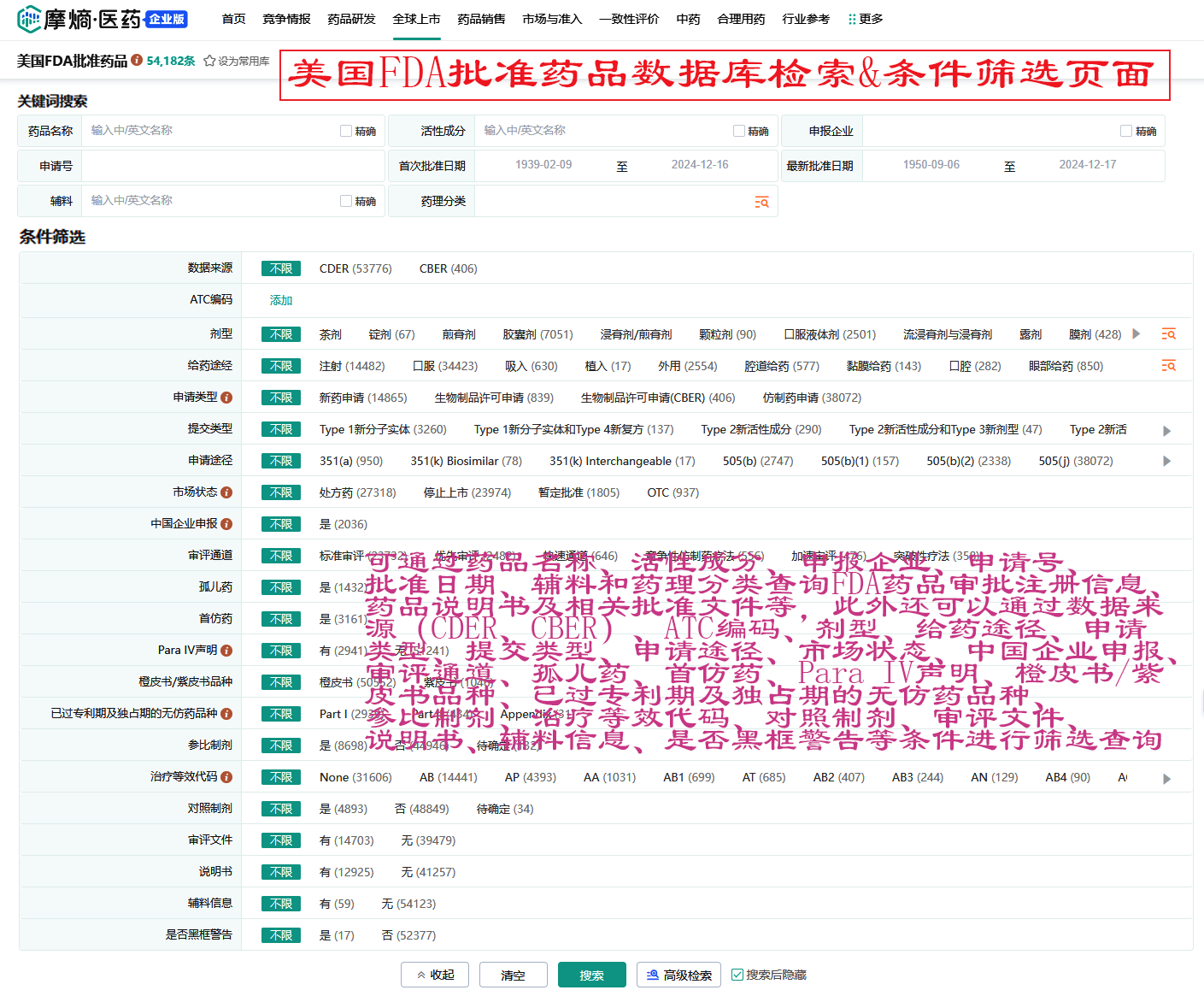
上图为摩熵医药的美国FDA批准药品数据库,可很便捷查阅并筛选其FDA批准药品的类信息。
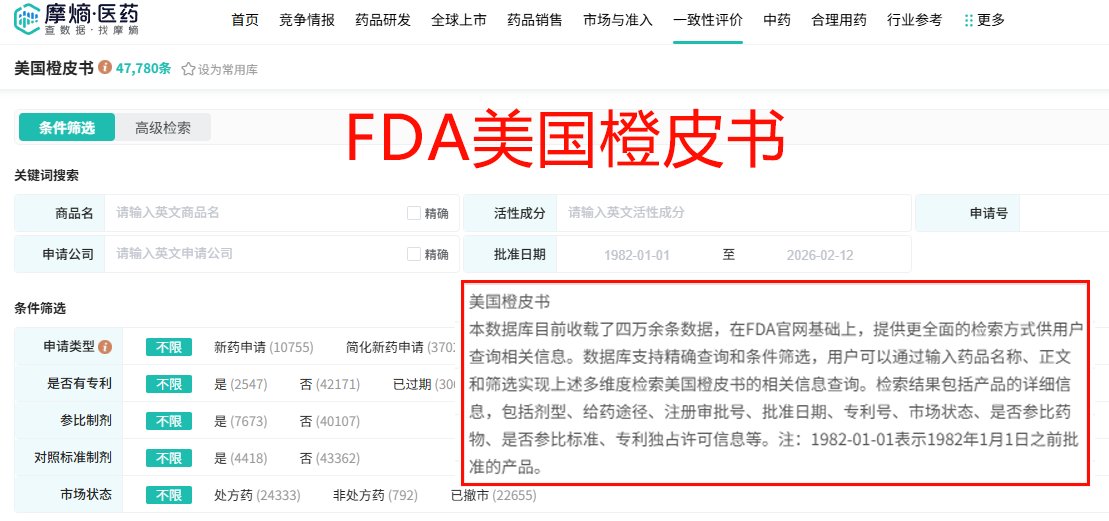
理解药品的治疗等效性是仿制药开发的核心前提,而橙皮书(Orange Book)正是这一领域的权威指南。其全称为《经治疗等效性评价批准药品》(Approved Drug Products with Therapeutic Equivalence Evaluations),自1980年首版发布以来,已成为全球仿制药产业的风向标。该数据库主要包含四类信息:具有治疗等效性评价的处方药、部分特殊OTC药品、根据FD&C法案第505条批准的生物制品,以及已退市或仅供特定用途的药品记录。其核心价值在于通过“治疗等效性代码”(Therapeutic Equivalence Code, TE Code)对仿制药与原研药的可替代性进行评级。可通过FDA官网的专用搜索界面,按活性成分、商品名、申请号或专利号进行检索。对于深度研究者而言,第三方平台如摩熵医药提供了更强大的功能,支持将TE代码、专利信息与市场独占权进行关联分析,并能一键跳转至相关企业的全景视图,适用于立项可行性评估与知识产权布局。
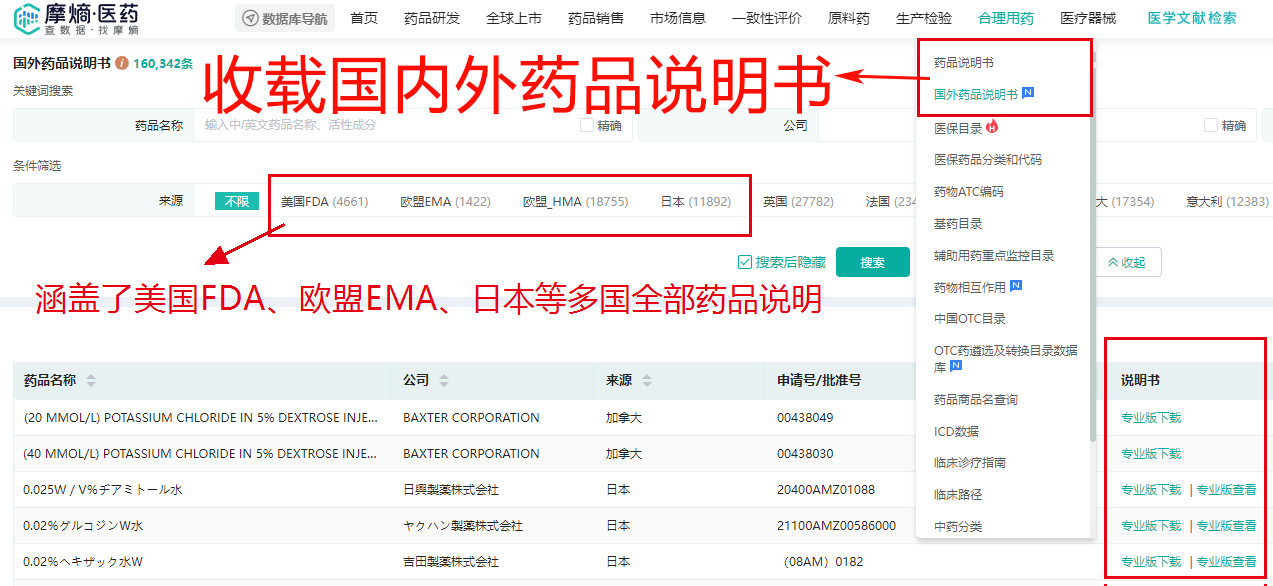
药品说明书是临床实践与药物警戒的基石,其内容完整性和可及性至关重要。FDA要求所有获批药品提交结构化产品标签(Structured Product Labeling, SPL),形成标准化电子文档。目前,公众可通过三大主流平台获取说明书信息:FDALabel、DailyMed和Drugs@FDA。FDALabel是FDA官方的SPL存储库,适合需要下载归档原始文件的用户;DailyMed由美国国家医学图书馆(NLM)运营,整合了FDA提交的所有标签数据,其界面友好,更新及时,适合快速查阅最新版说明书;而Drugs@FDA则提供了最全面的审批背景资料,除说明书外,还包含审评报告、CMC信息及完整的审批历史,是进行深度学术研究与竞品分析的首选。值得注意的是,由于网络访问限制,国内如面临加载缓慢的问题,可使用摩熵医药等本地化数据库作为补充,这些平台不仅实现了数据镜像,还通过关联将说明书中的关键信息与专利、临床试验等数据打通。
在药品研发的延伸领域,绿皮书(Green Book)与辅料数据库(Inactive Ingredient Database, IID)提供了不可或缺的专业支持。绿皮书,即FDA批准的动物用药目录,收录了用于宠物及家畜的兽药产品信息。该数据库对于探索国内外上市差异、发现潜在引进品种具有重要价值。例如,通过检索可发现溴化钾(Potassium Bromide)已被批准用于控制犬类癫痫发作,但在中国尚未获得上市许可,这为宠物药研发企业指明了差异化竞争的方向。辅料数据库(IID)则为制剂开发者提供了非活性成分的安全用量参考。该数据库列出了已获批药品中使用的非活性成分、其UNII编号、CAS号、给药途径,并明确标注了单剂量最大含量和日最大暴露量等关键参数。其官方入口位于FDA官网“Drugs”→“Drug Approvals and Databases”下的“Inactive Ingredient Search”。值得注意的是该数据库中标注的“Maximum potency”仅为当前已批准产品中的最高用量记录,并非绝对安全阈值。随着新产品的获批,该数值会动态更新,因此不能将其视为不可逾越的上限,而应结合毒理学数据进行综合评估。
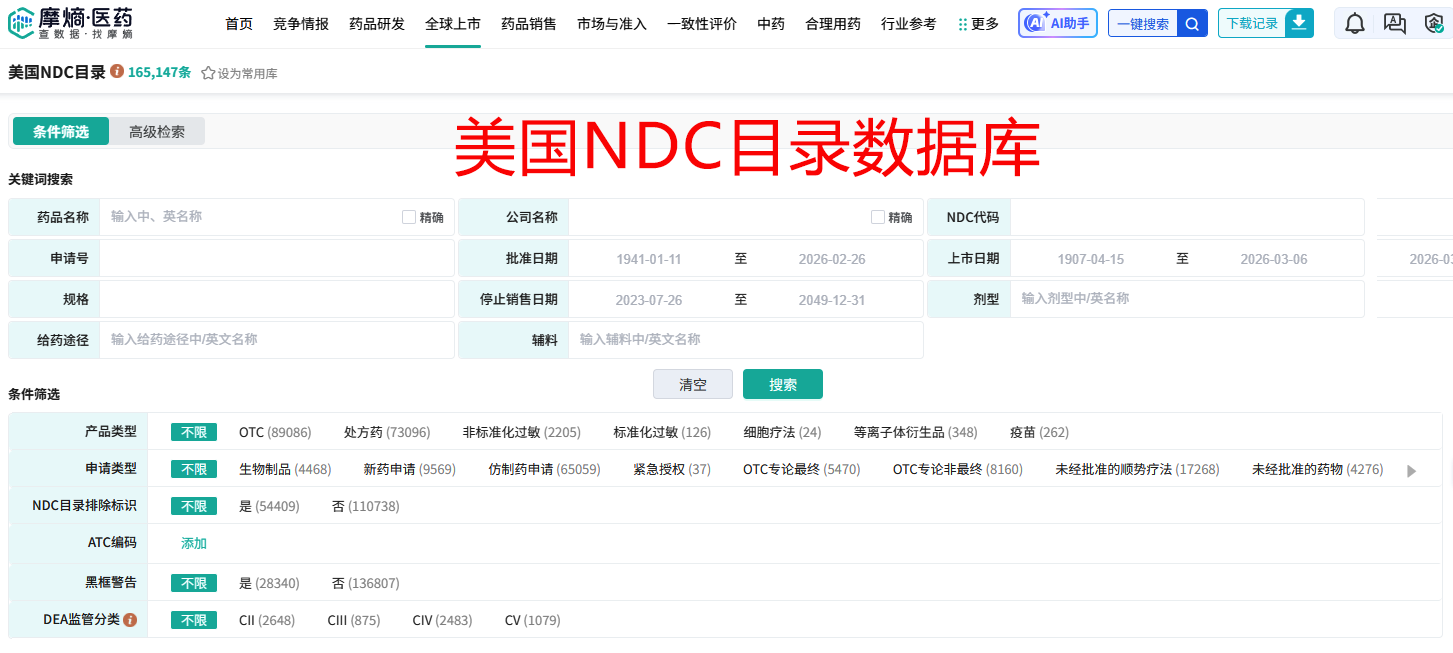
另外值得说一下,美国NDC药品代码。国家药品代码(National Drug Code, NDC)是美国联邦法律规定的药品法定编码,由10至11位数字组成,分为三段:标签商代码(Labeler Code)、产品代码(Product Number)和包装代码(Package Size)。该编码体系覆盖了所有在美国上市的处方药与非处方药成品制剂,是连接药品物理实体与其监管信息的关键纽带。NDC目录由FDA维护,收录了药品的商品名与通用名、活性成分、剂型、规格、生产商、上市状态以及OTC专论编号等关键信息。官方查询路径为:访问FDA官网,依次点击“Drugs”→“Drug Approvals and Databases”→“National Drug Code Directory”。对于需要进行跨国比较或批量数据分析的人群,推荐使用摩熵医药等集成化平台,其提供多条件筛选、历史版本追溯及与欧盟、日本等市场的横向对比功能,显著提升工作效率。
以上,就是FDA一些数据核心应用。官方数据库确保了信息的权威性与时效性,而专业的第三方平台则通过数据整合、多语言支持和高级分析功能,解决了访问障碍与操作复杂性问题。在典型应用场景中,仿制药立项可结合橙皮书与NDC目录锁定参比制剂;辅料选择可依托IID数据库优化配方,减少不必要的毒理投入;国际市场布局则可通过绿皮书挖掘海外成熟但国内空白的潜力品种。从业者应持续关注其技术演进,将结构化查询能力内化为核心竞争力。
随机推荐

