
6
0
AI临床试验管理系统项目开发的框架及思路!很实用!
如何开发一个基于数字化的临床试验管理系统呢?下面笔者根据摩熵医药平台对 CRO/CDMO企业开发的数字化临床试验管理系统案例,提炼了其主要项目的主要框架及一些思路,供大家一览,希望对大家有所帮助。
推荐指数:
详细信息
AI临床试验管理系统项目开发的框架及思路!很实用!
【某CRO/CDMO企业】基于数字化的临床试验管理系统项目方案
临床研究管理软件(CTMS)是一个专为药厂新药研发部门、有临床研究功能的独立的新药研究单位以及合同研究组织(CRO)提供的临床研究项目管理工具。一个功能全面的CTMS对整个临床试验中所涉及的人员、沟通、预算、进度、费用、文档以及申报等进行管理和控制,使管理者方便及时的掌握试验进展情况。
那么如何开发一个基于数字化的临床试验管理系统呢?下面笔者根据摩熵医药平台对 CRO/CDMO企业开发的数字化临床试验管理系统案例,提炼了其主要项目的主要框架及一些思路,供大家一览,希望对大家有所帮助。
一、项目背景
1.1 临床试验管理的挑战与机遇
临床试验是新药研发的核心环节,也是成本最高、周期最长、风险最大的阶段。据Tufts CSDD统计,一项临床试验平均成本约数千万美元,周期长达7-8年。随着创新药研发加速、临床试验数量激增,传统的纸质化、人工化临床试验管理模式已难以为继。
从药物类型维度来看,不同类型临床试验的管理特点:
①化学药临床试验:相对成熟,方案设计、统计分析方法有标准路径。重点关注:BE试验设计、剂量递增研究、确证性试验的统计考量。
②生物药临床试验:面临免疫原性评估、伴随诊断开发、生物标志物监测等特殊挑战。PK/PD关系更为复杂。
③中药临床试验:需兼顾中医证候评价与西医指标评价,建立中西医双终点评价体系。真实世界研究方法日益重要。
④ 细胞与基因治疗临床试验:面临独特挑战:长期随访需求、安全性监测复杂、剂量摸索困难、免疫反应评估等。风险控制计划尤为关键。
⑤寡核苷酸药物临床试验:需关注肝脏毒性监测、肾脏安全性评估、特殊不良事件的识别与归因。
1.2 行业痛点与情报需求
①项目进度管理困难:多中心协同效率低,中心多、沟通链条长、反馈慢。进度不透明,各中心、各阶段进度难以实时掌握。里程碑追踪繁琐,关键节点提醒依赖人工。资源冲突,研究者、CRC/CRA资源协调困难。
②文档管理混乱:方案、ICF等重要文档版本混乱。伦理批件、合同等关键文档追溯困难。监查报告、SAE报告等积累难以系统利用。文件传输依赖邮件,缺乏统一平台。
二、业务痛点
2.1 项目进度管理困难
①多中心协同效率低:中心多、沟通链条长、反馈慢。
②进度不透明:各中心、各阶段进度难以实时掌握。
③里程碑追踪繁琐:关键节点提醒依赖人工。
④资源冲突:研究者、CRC/CRA资源协调困难。
2.2 文档管理混乱
①重要文档版本混乱:方案、ICF等重要文档版本混乱。
②关键文档追溯困难:伦理批件、合同等关键文档追溯困难。
③报告积累难以利用:监查报告、SAE报告等积累难以系统利用。
④缺乏统一平台:文件传输依赖邮件,缺乏统一平台。
2.3 数据质量控制效率低
①EDC数据人工审核工作量大:E DC数据人工审核工作量大。
②数据疑问创建与解决流程冗长:数据疑问创建与解决流程冗长。
③偏离方案管理不及时:偏离方案(PD)管理不及时。
④质量风险识别滞后:质量风险识别滞后。
三、解决方案与技术实现
3.1 总体技术架构
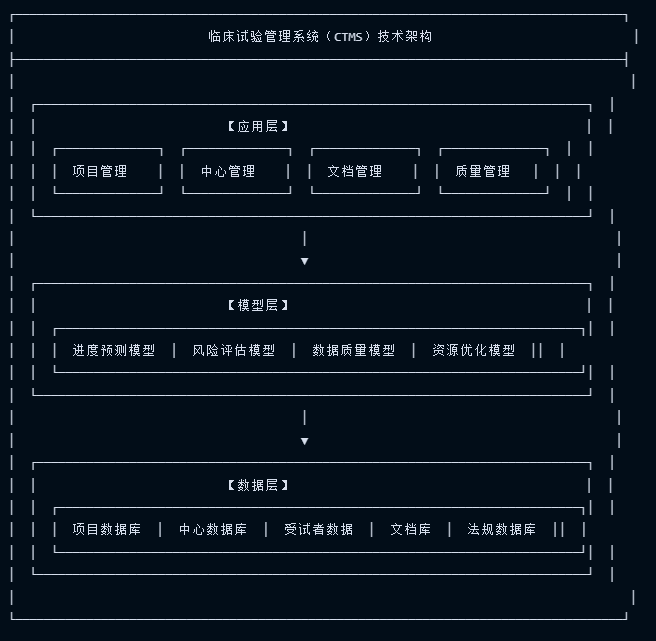
图源:摩熵医药
3.2 模块一:项目全流程管理

图源:摩熵医药
3.3 模块二:智能监查与质量管理
3.3.1 远程智能监查
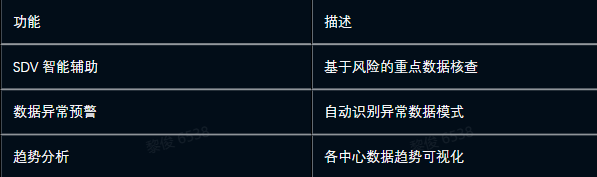
3.3.2 质量风险管理
①风险识别:基于历史数据的风险因素识别
②风险评估:关键数据和关键流程的风险等级
③ 风险控制:风险控制措施跟踪
3.4 模块三:文档与合规管理
3.4.1 TMF文档管理
①文档清单自动生成:根据方案类型生成必备文档清单
②文档状态追踪:缺失文档自动预警
③版本管理:文档版本追溯
3.4.2 审计追踪
① 操作日志完整记录
② 变更追溯:任何数据修改均可追溯
③审计准备:一键导出审计所需文件
四、价值成果
4.1 效率提升
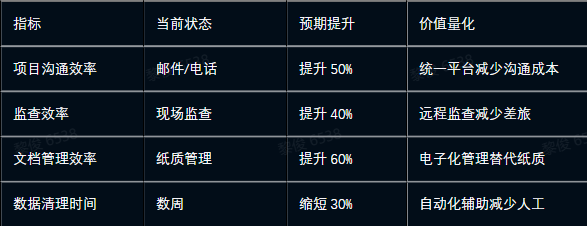
4.2 质量提升
① 临床试验数据质量显著提升
② 合规性增强,满足GCP核查要求
③ 风险前置识别,减少质量事故
4.3 战略价值
①缩短临床试验周期,加速药物上市
② 降低临床试验成本
③ 积累项目数据资产,形成知识复用
五、项目风险与应对策略
5.1 系统集成风险
风险描述:与EDC、IWRS等系统集成困难。
应对策略:
①开放API接口支持集成
②采用标准数据交换格式
③ 分阶段实施集成
5.2 数据安全风险
风险描述:临床数据涉及受试者隐私。
应对策略:
①数据脱敏处理
②严格的权限管理
③ 符合法规的数据保护措施
六、项目建设周期
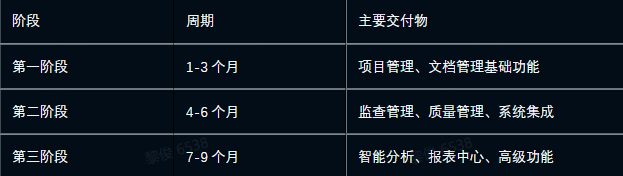
七、算力需求推荐方案
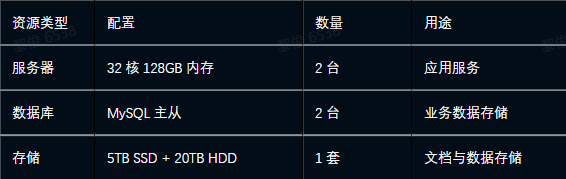
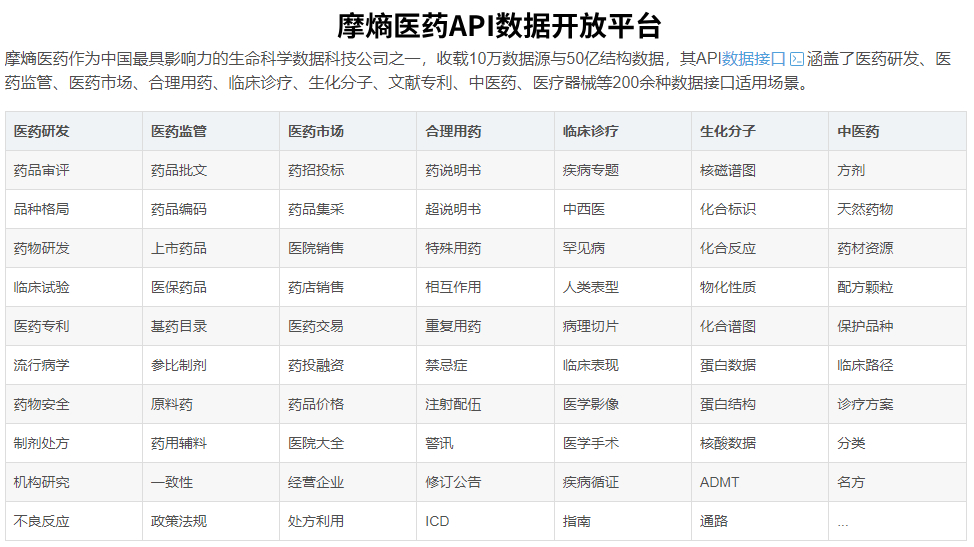
最后再提一下,关于项目方案中的一些标准化数据信息,除了购买摩熵医药的数据集外,其实还可以接入其API接口(例如在下图展示的摩熵医药数据分类表格),对于快速搭建,这样相对省心很多。
随机推荐
最新推荐

